

5 étapes pour l'optimisation de l'image :
Recherche des contre-indications.
Information du patient sur les modalités de l'examen pour limiter son anxiété (débit cardiaque) et le sensibiliser à l'importance d'une immobilité stricte.
Evaluer sa capacité d'apnée pour adapter les paramètres d'acquisition.
Pose d'une voie veineuse au pli du coude (cathéter 16G) ; pour l'exploration de l'aorte thoracique ou des troncs supra-aortiques, on préférera le bras droit pour éviter d'éventuels artéfacts dus au passage dans le tronc veineux innominé.
![]() Adapter
la position du patient et l'antenne utilisée au territoire vasculaire exploré:
Adapter
la position du patient et l'antenne utilisée au territoire vasculaire exploré:
| Tête et cou : | décubitus dorsal, bras le long du corps - Antenne tête, antenne tête-cou |
| Thorax - Abdomen : | décubitus dorsal, bras relevés (évite les artéfacts de repliement) - Antenne corps en réseau phasé. |
| Membres inférieurs : | décubitus dorsal, drap sous les jambes (axes vasculaires dans le même plan). Antenne corps en réseau phasé, antenne rachis ou spécifique (flexible et adaptable). |
Pourquoi injecter ?
L'injection intra veineuse d'un agent de contraste paramagnétique (Gadolinium) raccourcit le T1 du sang (de 1200 à 100 ms), ce qui accentue la différence de signal entre le compartiment vasculaire et les tissus environnants (graisse, muscle) créant ainsi l'angiogramme. (figure 1).
 |
Figure 1 : Courbes de relaxation T1 de différents tissus en fonction du temps. |
Contrairement aux autres techniques d'ARM (temps de vol et contraste de phase), l'ARM avec injection de produit de contraste évite les artéfacts de flux et de saturation.
| Dose : | La dose la plus habituellement utilisée est de 0,1 mmol/kg, cependant, certaines indications peuvent nécessiter jusqu'à 0,3 mmol/kg en plusieurs injections ; en particulier pour les membres inférieurs. |
| Débit : | Injection en bolus à un débit de 2 ml/s le plus souvent manuellement, et, si disponible, à l'aide d'un injecteur automatique suivi dans tous les cas d'un flush de solution saline. |
| Délai : | Paramètre primordial de la qualité de l'ARM. Il est nécessaire de déterminer le "temps de transit" vasculaire pour obtenir une présence maximale et homogène du produit de contraste dans le vaisseau étudié durant l'acquisition des lignes centrales de l'espace de Fourier (Espace k). |
![]() 2
méthodes permettent d'évaluer ce temps de transit :
2
méthodes permettent d'évaluer ce temps de transit :
- Dose Test : Injection de 2 ml de Gadolinium combinée à l'acquisition 2D toutes les secondes d'une section du vaisseau exploré afin d'évaluer le délai de réhaussement du vaisseau .
- Détection automatique (type SmartPrep TM de GE) : synchronisation automatique par l'imageur qui lance l'acquisition EG3D une fois que le seuil de réhaussement pré-fixé dans le vaisseau exploré est atteint.

![]() 2
méthodes permettent d'obtenir une séquence avec réhaussement vasculaire optimal:
2
méthodes permettent d'obtenir une séquence avec réhaussement vasculaire optimal:
- FluoroIRM : Séquence 2D réalisée avant la séquence EG3D, au debut de l'injection du produit de contraste, permettant au médecin de visualiser " en direct " le réhaussement du vaisseau exploré et donc de lancer l'acquisition 3D au moment opportun.
- "3D TRICK" (Time Resolved Imaging on Contrast Kinetics) : Technique d'avenir de traitement de l'espace de Fourier permettant une acquisition 3D ultra rapide (2 sec) de façon successive, et ainsi, d'individualiser les différents temps d'injection.
![]() Utilisation d'un aimant d'au moins 1Tesla.
Utilisation d'un aimant d'au moins 1Tesla.
Séquence Echo de Gradient 3D
La technique en EG "spoilé" (suppression de l'aimantation transversale résiduelle assurant une pondération T1 "pure") est utilisée car elle répond aux impératifs de rapidité de l'ARM. Cette séquence est réalisée durant une apnée.
Les différents paramètres sont toujours un compromis entre la résolution spatiale, nécessaire à la caractérisation des lésions, et la résolution temporelle nécessaire à l'imagerie du premier passage du produit de contraste :
| Temps d'Echo (TE) | minimum (<3ms): Diminution des artéfacts de flux. |
| Temps de répetition (TR) | court : Principal élément de la diminution du temps d'acquisition (TA). Saturation des tissus stationnaires. |
| FOV | Rectangulaire (diminution du TA). |
L'examen commence toujours par un repérage en T1 Spin Echo ou directement en EG2D et éventuellement des séquences morphologiques selon la pathologie explorée.
L'acquisition en EG3D-gadolinium des coupes "natives" se fait selon l'axe du vaisseau déroulé pour en visualiser le maximum dans un minimum de coupes. Les coupes natives seront CORONALES pour l'aorte abdominale, les rénales, les carotides, les membres inférieurs; SAGITTALES pour l'aorte thoracique, ou AXIALES dans certains cas d'exploration des artères sous clavières.
Comment aborder l'ARM sans parler de l'espace k (ou "espace de Fourier") ?
L'espace k est composé d'un encodage en fréquence de l'ensemble des signaux recueillis pendant la séquence. L'analyse de l'espace k ne peut donner une image qu'après l'application de la "transformée de Fourier" (formule mathématique complexe).
En pratique, il faut retenir que dans l'espace k, les basses fréquences, situées au centre, déterminent le contraste de l'image et que les hautes frequences, situées en périphérie déterminent sa résolution spatiale.
Il existe différentes techniques d'acquisition de l'espace k (figure 2). En Angio-IRM, on s'intéresse principalement à sa partie centrale, dont l'acquisition devra coincider au mieux avec le pic de contraste (figure 3).
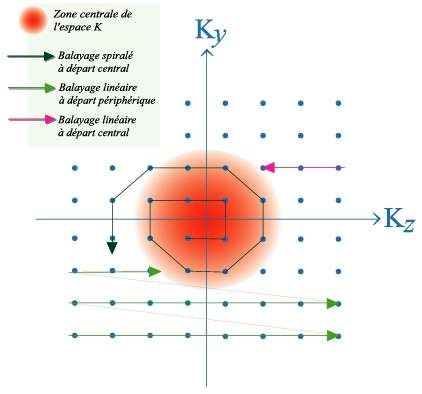 |
Figure 2 : Représentation schématique de l'espace K pour une matrice 8 * 8 : Trois modes d'échantillonage du signal. |
 |
Figure 3 : Concordance des modes d'échantillonage de l'espace K avec l'injection. |
Le balayage elliptique de l'espace k en partant de son centre permet d'obtenir des images avec un contraste maximal en améliorant la résolution spatiale. Ex: Exploration des troncs supra aortiques.
Enfin, certaines techniques permettent de n'acquérir que partiellement l'espace k, afin d'améliorer soit la résolution temporelle ("Half Fourier"), soit la résolution spatiale ("Zero Filling").
Ces notions permettent en pratique d'adapter la séquence utilisée au territoire vasculaire exploré et à sa cinétique de réhaussement.
Etape essentielle
![]() Etude des images natives
Etude des images natives
Fondamentale, elle permet d'analyser la lumière vasculaire, sa paroi et son environnement. Cette étude se fait au mieux en mode "ciné-loop".
![]() Reformations et reconstructions
Reformations et reconstructions
MIP (Multiplanar Intensity Projection) : Après sélection des voxels d'intensité maximale, on réalise en temps réel et dans tous les plans de l'espace, de multiples projections qui aboutissent à la matérialisation d'un angiogramme.
Exemple de projection MIP où la projection des deux images de gauche aboutit à une image "MIP" telle qu'on pourrait l'obtenir au moyen d'une angiographie par rayons X.
Reconstruction surfacique et volumique : Un fenêtrage adapté permet d'obtenir deux types de vues:
.Endoluminales (endoscopie vasculaire virtuelle ou "VIE")
.Exoluminales (image "3D") - Technique de soustraction C'est la soustraction d'une acquisition sur une autre permettant d'améliorer la visualisation de l'angiogramme en supprimant le signal des tissus avoisinnants.